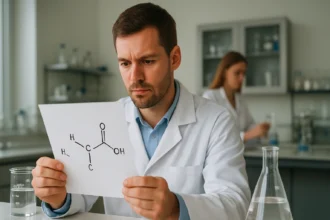
A kémiai világban minden folyamat alapját a különböző anyagok közötti kölcsönhatások képezik. Amikor egy új gyógyszer kifejlesztéséről hallunk, vagy éppen arról, hogy hogyan működik a fotoszintézis növényeinkben, valójában bonyolult kémiai táncról beszélünk, ahol minden egyes résztvevőnek meghatározott szerepe van. Ez a világ sokkal közelebb áll hozzánk, mint gondolnánk – már reggeli kávénk elkészítése során is számtalan kémiai átalakulás zajlik.
A reagáló anyagok azok a kiindulási vegyületek, amelyek részt vesznek egy kémiai reakcióban, és átalakulnak új termékekké. Ezek az anyagok képezik minden kémiai folyamat alapkövét, legyen szó akár ipari gyártásról, biológiai folyamatokról vagy mindennapi jelenségekről. A téma megértése különböző szemszögekből közelíthető meg: a molekuláris szintű változásoktól kezdve a gyakorlati alkalmazásokig.
Az elkövetkező sorok során betekintést nyerhetsz abba, hogyan működnek ezek a folyamatok, milyen tényezők befolyásolják őket, és miért olyan fontosak mindennapi életünkben. Megismerheted a különböző típusú reagáló anyagokat, azok viselkedését, valamint gyakorlati példákon keresztül láthatod, hogyan alkalmazhatod ezt a tudást.
Mi tesz egy anyagot reagálóvá?
A kémiai reakciók világában nem minden anyag viselkedik egyformán. Egyes vegyületek rendkívül aktívak és könnyen lépnek reakcióba másokkal, míg mások stabilabbak és különleges körülményeket igényelnek az átalakuláshoz.
Az elektronszerkezet játssza a főszerepet abban, hogy egy anyag mennyire hajlamos reagálni. A külső elektronhéjon található elektronok száma és elrendeződése határozza meg, hogy egy atom vagy molekula milyen könnyen alakít ki kötéseket másokkal. Az alkálifémek például rendkívül reaktívak, mert külső héjukon egyetlen elektron található, amelyet könnyen leadnak.
A molekulák térbeli szerkezete szintén döntő fontosságú. Egy egyszerű példával élve: a gyémánt és a grafit egyaránt szénből áll, mégis teljesen eltérő tulajdonságokkal rendelkeznek. A gyémánt rendkívül stabil szerkezete miatt nehezen reagál, míg a grafit sokkal reaktívabb formája a szénnek.
A reakciók hajtóerői
Energetikai szempontok
Minden kémiai reakció mögött energetikai változások állnak. A reagáló anyagok energiaszintje és a termékek energiaszintje közötti különbség határozza meg, hogy egy reakció spontán módon végbemegy-e vagy külső energiabevitelre van szükség.
Az aktiválási energia fogalma kulcsfontosságú a megértésben. Ez az az energiaküszöb, amelyet át kell lépni ahhoz, hogy a reakció elkezdődhessen. Képzeljük el úgy, mint egy hegyet, amelyet meg kell mászni ahhoz, hogy a túloldalra jussunk. Minél magasabb ez a "hegy", annál nehezebb elindítani a reakciót.
A katalizátorok szerepe éppen ebben rejlik: alternatív, alacsonyabb energiájú utat biztosítanak a reakció számára. Ezek az anyagok nem fogynak el a folyamat során, csupán megkönnyítik az átalakulást.
Termodinamikai tényezők
A termodinamika törvényei meghatározzák, hogy egy reakció energetikailag kedvező-e. Az entalpia és az entrópia változása együttesen dönti el egy folyamat spontaneitását.
"A természet mindig a legalacsonyabb energiaállapot felé törekszik, és ezt a törekvést használjuk ki a kémiai szintézisekben."
Az exoterm reakciók során energia szabadul fel, míg az endoterm reakciók energiát igényelnek. A mindennapi életben számos példát találunk mindkettőre: a tűz égése exoterm, míg a fotoszintézis endoterm folyamat.
Reagáló anyagok típusai és jellemzőik
A kémiai világban a reagáló anyagokat különböző szempontok szerint csoportosíthatjuk. Ez a kategorizálás segít megérteni viselkedésüket és előre jelezni reakcióikat.
Szervetlen reagensek
A szervetlen vegyületek széles spektrumot ölelnek fel a egyszerű sóktól a komplex fémkomplexekig. Ezek az anyagok gyakran ionos karakterűek, ami különleges tulajdonságokat kölcsönöz nekik.
Az erős savak és bázisok tipikus példái a reaktív szervetlen anyagoknak. A kénsav, sósav vagy nátrium-hidroxid mind olyan vegyületek, amelyek vízes oldatban teljesen disszociálnak, ezáltal erőteljes kémiai változásokat képesek előidézni.
A fémek reaktivitása széles skálán mozog. Az alkálifémek (nátrium, kálium) víz jelenlétében is hevesen reagálnak, míg a nemesfémek (arany, platina) rendkívül stabilak és csak különleges körülmények között lépnek reakcióba.
| Fémcsoport | Reaktivitás | Tipikus reakciók |
|---|---|---|
| Alkálifémek | Nagyon magas | Víz, oxigén, halogének |
| Alkáliföldfémek | Magas | Víz (lassan), savak |
| Átmeneti fémek | Közepes | Savak, oxidálószerek |
| Nemesfémek | Alacsony | Erős oxidálószerek |
Szerves reagensek
A szerves kémia világában a reagáló anyagok sokfélesége még nagyobb. A szénvázas molekulák végtelen variációi különböző funkciós csoportokkal rendelkeznek, amelyek meghatározzák reakciókészségüket.
Az alkoholok, aldehidek, ketonok mind jellegzetes reakciókra képesek. Az alkoholok például könnyen oxidálódnak aldehidekké vagy ketonokká, míg az aldehidek tovább oxidálódhatnak savakká.
A funkciós csoportok jelenléte nem csak a reaktivitást, hanem a szelektivitást is befolyásolja. Egy molekulában több funkciós csoport is lehet, és ezek eltérő körülmények között különbözőképpen viselkedhetnek.
Koncentráció és reakciósebesség kapcsolata
A reagáló anyagok koncentrációja alapvetően befolyásolja a reakció sebességét. Ez a kapcsolat nem mindig lineáris, és megértése kulcsfontosságú a reakciók irányításában.
A reakciókinetika törvényei szerint a legtöbb reakció sebessége arányos a reagáló anyagok koncentrációjával. Ha megduplázzuk egy reaktáns koncentrációját, gyakran a reakciósebesség is megduplázódik, bár ez nem minden esetben igaz.
Az elsőrendű reakciók esetében a sebesség egyenesen arányos egy reaktáns koncentrációjával. A radioaktív bomlás tipikus példája ennek: a bomlási sebesség mindig arányos a jelenlévő radioaktív atomok számával.
Másodrendű reakcióknál a helyzet bonyolultabb. Itt a sebesség két reaktáns koncentrációjának szorzatával arányos, vagy egy reaktáns koncentrációjának négyzetével. Ez azt jelenti, hogy kis koncentrációváltozások is jelentős hatással lehetnek a reakciósebességre.
"A koncentráció és a reakciósebesség közötti összefüggés megértése lehetővé teszi a kémiai folyamatok precíz szabályozását az iparban és a laboratóriumban egyaránt."
Hőmérséklet hatása a reaktivitásra
A hőmérséklet emelése általában növeli a reakciók sebességét, de ez a hatás nem egyforma minden esetben. Az Arrhenius-egyenlet matematikailag leírja ezt a kapcsolatot.
Magasabb hőmérsékleten a molekulák gyorsabban mozognak, gyakrabban ütköznek egymással, és az ütközések energiája is nagyobb. Ez azt jelenti, hogy több molekula rendelkezik az aktiválási energia leküzdéséhez szükséges energiával.
Gyakorlati szempontból ez rendkívül fontos. Az ételek főzése során a hőmérséklet emelése felgyorsítja a kémiai átalakulásokat, amelyek az ízek és textúrák kialakulásáért felelősek. Hasonlóképpen, az ipari folyamatokban a hőmérséklet szabályozásával optimalizálhatjuk a termelést.
Gyakorlati példa: Cukor karamellizálása
A cukor karamellizálása kiváló példája annak, hogyan befolyásolja a hőmérséklet a kémiai reakciókat:
🔥 150°C alatt: A cukor kristályos szerkezete megmarad, nincs jelentős kémiai változás
🔥 160-170°C: Elkezdődik a dehidratáció, a cukor molekulák vízkilépés mellett átrendeződnek
🔥 180-190°C: Intenzív karamellizáció, komplex aromás vegyületek keletkeznek
🔥 200°C felett: Túlzott bomlás, keserű ízű vegyületek dominálnak
Ez a folyamat jól mutatja, hogy a hőmérséklet nem csak a reakciósebesség, hanem a reakcióutak irányítása szempontjából is kulcsfontosságú.
Katalizátorok és inhibitorok szerepe
A katalizátorok olyan anyagok, amelyek felgyorsítják a kémiai reakciókat anélkül, hogy maguk megváltoznának. Működésük megértése forradalmasította a modern kémiát és lehetővé tette számos ipari folyamat hatékonyságának növelését.
Homogén és heterogén katalizátorok
A homogén katalizátorok ugyanabban a fázisban vannak jelen, mint a reagáló anyagok. Tipikus példa erre a savkatalizált észteresítés, ahol a kénsav katalizátor oldatban van a reaktánsokkal együtt.
A heterogén katalizátorok másik fázisban találhatók. A leggyakoribb példák a szilárd felületű katalizátorok, amelyeken gázfázisú vagy folyadékfázisú reakciók játszódnak le. Az autók katalizátorában platina és palládium segíti a káros kipufogógázok ártalmatlanítását.
Enzimkatalizis
Az élő szervezetekben az enzimek látják el a katalizátor szerepét. Ezek a fehérjemolekulák rendkívül specifikusak és hatékonyak. Egy enzim gyakran milliószor gyorsítja fel az általa katalizált reakciót.
"Az enzimek működése olyan precíz, mint egy jól beállított óramű: minden egyes lépés pontosan a megfelelő időben és helyen történik."
Az enzimkatalizis különlegessége a szubsztrátspecifikusságban rejlik. Minden enzim csak bizonyos típusú molekulákat ismer fel és alakít át, ami lehetővé teszi a komplex biológiai folyamatok pontos szabályozását.
Oldószerek hatása a reakciókra
Az oldószer választása gyakran döntő fontosságú egy kémiai reakció sikerében. Az oldószer nem pusztán közeg, hanem aktív résztvevője lehet a folyamatnak.
A poláris oldószerek (víz, alkoholok) stabilizálják az ionos átmeneti állapotokat, ezáltal kedvezővé teszik az ionos mechanizmusú reakciókat. A víz például kiváló oldószer a sav-bázis reakciókhoz, mert képes szolvatálni mind a pozitív, mind a negatív ionokat.
Az apoláris oldószerek (hexán, benzol) inkább a radikálos vagy molekuláris mechanizmusú reakciókat támogatják. Ezekben az oldószerekben az ionos intermedierek instabilak, így a reakciók más útvonalakon mennek végbe.
| Oldószer típus | Jellemzők | Alkalmas reakciók |
|---|---|---|
| Poláris protikus | Hidrogénkötés, ionszolvatáció | SN1, elimináció |
| Poláris aprotikus | Ionszolvatáció H-kötés nélkül | SN2, nukleofil addíció |
| Apoláris | Gyenge intermolekuláris erők | Radikálos, cikloaddíció |
Oldószerhatások gyakorlati szempontjai
A megfelelő oldószer kiválasztása nem csak tudományos, hanem gazdasági és környezeti szempontból is fontos. A zöld kémia egyik alapelve a környezetbarát oldószerek használata.
A víz mint oldószer egyre nagyobb figyelmet kap, mivel nem toxikus, olcsó és könnyen hozzáférhető. Sok hagyományosan szerves oldószerekben végzett reakciót sikerült vizes közegbe átvinni megfelelő adalékanyagok használatával.
Gyakori hibák reagáló anyagok használatában
A kémiai reakciók végrehajtása során számos hiba előfordulhat, amelyek a várt eredmény elmaradásához vagy nemkívánatos mellékterméket képződéséhez vezethetnek.
Sztöchiometriai hibák
Az egyik leggyakoribb probléma a nem megfelelő mólarányok használata. Ha egy reaktánsból túl keveset vagy túl sokat használunk, az hatással van a hozamra és a termék tisztaságára.
A limitáló reagensek azonosítása kulcsfontosságú. Ez az a reaktáns, amely elsőként fogy el a reakció során, és ezáltal meghatározza a maximálisan elérhető termékhozamot. A számítások során ezt mindig figyelembe kell venni.
Tisztasági problémák
A reagáló anyagok tisztasága jelentősen befolyásolja a reakció kimenetelét. A szennyeződések katalizálhatják vagy gátolhatják a kívánt reakciót, esetleg teljesen más irányba terelhetik azt.
"A kémiai tisztaság nem luxus, hanem alapvető követelmény a reprodukálható eredményekhez."
A víz jelenléte különösen problémás lehet vízmentes reakciók esetében. Sok szerves reakció érzékeny a nedvességre, és már kis mennyiségű víz is megváltoztathatja a reakció mechanizmusát.
Időzítési problémák
A reagensek hozzáadásának sorrendje és időzítése kritikus lehet. Egyes reaktánsok túl gyors hozzáadása lokális túlmelegedést vagy nemkívánatos mellékreakciókat okozhat.
A kvench (reakció megszakítása) helytelen időzítése szintén problémás lehet. Ha túl korán megszakítjuk a reakciót, nem érjük el a teljes konverziót. Ha túl későn, degradációs termékek keletkezhetnek.
Biológiai rendszerekben zajló reakciók
Az élő szervezetekben zajló kémiai reakciók különleges körülmények között mennek végbe. A biológiai környezet számos egyedi kihívást és lehetőséget teremt.
Fiziológiás körülmények
A biológiai reakciók általában enyhe körülmények között zajlanak: közel semleges pH, mérsékelt hőmérséklet és vizes közeg. Ezek a korlátok különleges stratégiákat igényelnek a hatékony katalízis érdekében.
Az enzimek evolúciója során olyan szerkezeteket alakítottak ki, amelyek optimálisan működnek ezekben a körülményekben. Az aktív hely mikrokörnyzete gyakran jelentősen eltér a külső környezettől, lehetővé téve a hatékony katalízist.
Metabolikus útvonalak
A metabolizmus során számos egymást követő reakció zajlik, ahol az egyik reakció terméke a következő reakció reagáló anyaga lesz. Ez a kapcsolódó reakciók rendszere lehetővé teszi a hatékony energiaátalakítást és anyagcserét.
A glikolízis során például a glükóz tíz lépésben alakul át piruvattá, és minden egyes lépésben specifikus enzimek katalizálják a reakciókat. Az egyes lépések finoman szabályozottak, hogy biztosítsák az optimális energiakinyerést.
"A biológiai rendszerek a kémiai reakciók mesterművei: minimális energiafelhasználással maximális hatékonyságot érnek el."
Ipari alkalmazások és nagy léptékű reakciók
Az ipari kémiai folyamatok során a reagáló anyagok viselkedésének megértése gazdasági és környezeti szempontból is kritikus fontosságú.
Folyamatoptimalizálás
A nagyüzemi gyártásban a kis hatékonyságjavítások is jelentős gazdasági előnyökkel járhatnak. A reaktánsok koncentrációjának, hőmérsékletének és nyomásának optimalizálása révén növelhető a hozam és csökkenthető a hulladékképződés.
A Le Chatelier-elv alkalmazása lehetővé teszi az egyensúlyi reakciók eltolását a kívánt irányba. Az ammónia szintézise során például magas nyomást és közepes hőmérsékletet alkalmaznak az egyensúly a termékek felé eltolásához.
Környezeti szempontok
A modern ipar egyre nagyobb figyelmet fordít a környezeti hatások minimalizálására. Az atom-gazdaságosság fogalma azt fejezi ki, hogy a reagáló anyagok atomjainak minél nagyobb hányada kerüljön be a kívánt termékbe.
A katalízis fejlesztése kulcsszerepet játszik ebben a törekvésben. Jobb katalizátorok használatával csökkenthető a melléktermékek képződése és javítható az energiahatékonyság.
Analitikai módszerek a reakciók követésére
A reagáló anyagok viselkedésének megértéséhez elengedhetetlen a reakciók pontos követése és elemzése.
Spektroszkópiai módszerek
Az NMR spektroszkópia lehetővé teszi a molekulák szerkezetének és a reakciók mechanizmusának részletes tanulmányozását. Valós időben követhetjük a reagáló anyagok eltűnését és a termékek megjelenését.
Az IR spektroszkópia különösen hasznos a funkciós csoportok változásainak követésére. Egy észteresítési reakció során például láthatjuk a karboxilsav C=O csúcsának eltűnését és az észter C=O csúcsának megjelenését.
Kromatográfiás technikák
A gázkromatográfia és folyadékkromatográfia lehetővé teszi a reakcióelegyek komponenseinek szétválasztását és mennyiségi meghatározását. Ez különösen fontos a reakciók hozamának és szelektivitásának meghatározásában.
Az HPLC (nagy hatékonyságú folyadékkromatográfia) segítségével nyomon követhetjük a reakció kinetikáját, meghatározva a reagáló anyagok koncentrációjának időbeli változását.
"A modern analitikai módszerek olyan betekintést nyújtanak a kémiai reakciókba, amelyről korábbi generációk csak álmodhattak."
Kinetikai vizsgálatok
A reakciókinetika tanulmányozása révén megérthetjük, hogy milyen tényezők befolyásolják a reakció sebességét. Ez az információ kulcsfontosságú a reakciókörülmények optimalizálásában.
A kezdeti sebesség módszere lehetővé teszi a reakciórend meghatározását úgy, hogy a kezdeti koncentrációkat változtatjuk és mérjük a kezdeti reakciósebességeket.
Gyakran Ismételt Kérdések
Miért változik a reagáló anyagok aktivitása az idővel?
A reagáló anyagok aktivitása többféle okból csökkenhet: bomlás, oxidáció, nedvességfelvétel vagy szennyeződések felhalmozódása miatt. A megfelelő tárolási körülmények (hűtés, inert atmoszféra, szárazság) segítenek megőrizni az aktivitást.
Hogyan lehet meghatározni a szükséges reagáló anyag mennyiségét?
A sztöchiometriai számítások alapján kell meghatározni a mólarányokat, figyelembe véve a reakció egyenletét. Mindig számolni kell a limitáló reagenssel, és gyakran kis felesleget alkalmaznak a teljes konverzió biztosítására.
Miért fontos a reagáló anyagok tisztasága?
A szennyeződések megváltoztathatják a reakció mechanizmusát, csökkenthetik a hozamot vagy nemkívánatos melléktermékeket eredményezhetnek. A reprodukálható eredményekhez konzisztens tisztaságú reagensek szükségesek.
Lehet-e ugyanazt a reagenst több reakcióban is használni?
Igen, sok reagens univerzális alkalmazású, de a reakciókörülményeket (hőmérséklet, oldószer, katalizátor) minden esetben a specifikus reakcióhoz kell igazítani az optimális eredmény érdekében.
Hogyan lehet biztonságosan kezelni a reaktív anyagokat?
A biztonságos kezelés magában foglalja a megfelelő védőfelszerelés használatát, a vegyszer biztonsági adatlapjának ismeretét, megfelelő tárolást és a veszélyes anyagok kezelésére vonatkozó protokollok betartását.
Mi a különbség a reagáló anyag és a katalizátor között?
A reagáló anyag átalakul a reakció során és beépül a termékbe, míg a katalizátor változatlan formában regenerálódik és újra felhasználható. A katalizátor csak a reakció sebességét befolyásolja, az egyensúlyi helyzetet nem.